



























Prepara tus exámenes y mejora tus resultados gracias a la gran cantidad de recursos disponibles en Docsity

Gana puntos ayudando a otros estudiantes o consíguelos activando un Plan Premium


Prepara tus exámenes
Prepara tus exámenes y mejora tus resultados gracias a la gran cantidad de recursos disponibles en Docsity
Prepara tus exámenes con los documentos que comparten otros estudiantes como tú en Docsity
Los mejores documentos en venta realizados por estudiantes que han terminado sus estudios
Estudia con lecciones y exámenes resueltos basados en los programas académicos de las mejores universidades
Responde a preguntas de exámenes reales y pon a prueba tu preparación

Consigue puntos base para descargar
Gana puntos ayudando a otros estudiantes o consíguelos activando un Plan Premium
Comunidad
Pide ayuda a la comunidad y resuelve tus dudas de estudio
Descubre las mejores universidades de tu país según los usuarios de Docsity
Ebooks gratuitos
Descarga nuestras guías gratuitas sobre técnicas de estudio, métodos para controlar la ansiedad y consejos para la tesis preparadas por los tutores de Docsity
Metano y aire para la combustión, aprovechamiento del metano
Tipo: Resúmenes
1 / 34

Esta página no es visible en la vista previa
¡No te pierdas las partes importantes!



























Alejandro Aguilar López Eammi Denisse Almaraz Varela Evangelina Barojas Rojas Brian Tagua C. Brenda Andrea Tovar Rocha
Materiales ideales El uso de materiales más activos para la combustión sin llama de hidrocarburos gaseosos son: ◦ (^) los metales nobles ◦ (^) los óxidos simples de metales de transición La principal desventaja de estos metales nobles tienen alto costo, son inestables a altas temperaturas y de poca disponibilidad. Los óxidos de metales de transición, aunque son menos costosos que los metales nobles, también presentan inestabilidad térmica y algunos tienen baja disponibilidad.
◦ (^) La oxidación de metano sobre óxido de magnesio puro o dopado con otros elementos como litio, hierro, cobalto y calcio. ◦ (^) El sistema litio-óxido de magnesio muestra mayor selectividad hacia etano y etileno, por acoplamiento oxidativo, que hacia dióxido de carbono por oxidación total. ◦ (^) Cuando el MgO se dopa con cobalto o hierro se da la oxidación total del metano promovida por el metal de transición. ◦ (^) La presencia de calcio en la superficie del óxido de magnesio aumenta de manera considerable la actividad para oxidación parcial de metano. El óxido de magnesio puro, usado frecuentemente como soporte de metales nobles por su alta estabilidad térmica, tiene alguna actividad para la oxidación total de metano en exceso de oxígeno.
Se investigó la combustión sin llama de mezclas pobres metano-aire, en un lecho fijo empacado con partículas de material activo obtenido por secado y calcinación del hidróxido de magnesio. Las suspensiones acuosas de hidróxido se prepararon a partir de óxido de magnesio grado industrial (conteniendo impurezas de calcio) y con óxidos de magnesio y de calcio grado reactivo. Se investigó el efecto de la relación oxígeno a metano, velocidad espacial, temperatura de calcinación y contenido de calcio sobre la actividad y estabilidad térmica.
Preparación Se prepararon suspensiones acuosas de una parte de sólido por cuatro de agua, con agitación mecánica durante 1.50 horas ◦ (^) Se separó el sedimento después de 12 horas y se secó en estufa a 125°C por 36 horas. ◦ (^) El sólido seco se compactó en una matriz de acero, se trituró y tamizó para conformar partículas con tamaños entre 2.00 y 2.36 mm que luego se calcinaron en aire durante 4 horas a 900, 1000 y 1100°C.
Instalación experimental ◦ (^) Se uso aire atmosférico y metano de alta pureza. ◦ (^) Para regular el flujo de mezcla reactiva metano- aire se fijó el caudal de metano y se ubicado después del mezclador, ◦ (^) un regulador de flujo másico total tipo hilo caliente dotado con interfaz de usuario y electrónica local, con una exactitud de ± 0.01 litros estándar por minuto. ◦ (^) La concentración de metano en la mezcla alimentada al reactor se midió con un analizador de gases tipo infrarrojo. ◦ (^) El calentamiento y control de temperatura se realizó mediante una resistencia eléctrica manejada con un control de temperatura multicanal con precisión de 0.1ºC.
Pruebas de actividad Se realizaron pruebas para investigar el efecto de ◦ (^) Adición de óxido de calcio (0.00, 0.25, 0.50 y 1.00% en peso) ◦ (^) Temperatura de calcinación (900, 1000 y 1100oC) ◦ (^) Velocidad espacial (23500, 83000, 120000, 154000 y 180000 h-1) ◦ (^) Exceso de oxígeno (mezclas aire-metano preparadas con 9.50, 5.00, 2.50 y 1.25% de metano en volumen).
Pruebas de estabilidad ◦ (^) La estabilidad del material a altas temperaturas y en condiciones de reacción, se investigó por los cambios presentados en superficie específica y cristalinidad. ◦ (^) El área superficial B.E.T. del material calcinado, antes y después de usarlo en la reacción de combustión, se determinó por adsorción de nitrógeno a 77K.
◦ (^) Previo a la medida del área todas las muestras se evacuaron por 3h a 300°C, para eliminar impurezas adsorbidas y humedad. ◦ (^) Se hicieron análisis por Difracción de Rayos X de polvos utilizando un equipo, filtro de Fe, K-∞ del Co (1.78897 nm). ◦ (^) Los ensayos se corrieron entre 30-80° utilizando un paso de 0.037° y un tiempo en cada punto de 0.50 segundos. Los análisis se hicieron a las muestras de sólido calcinado, antes y después de la reacción de combustión.
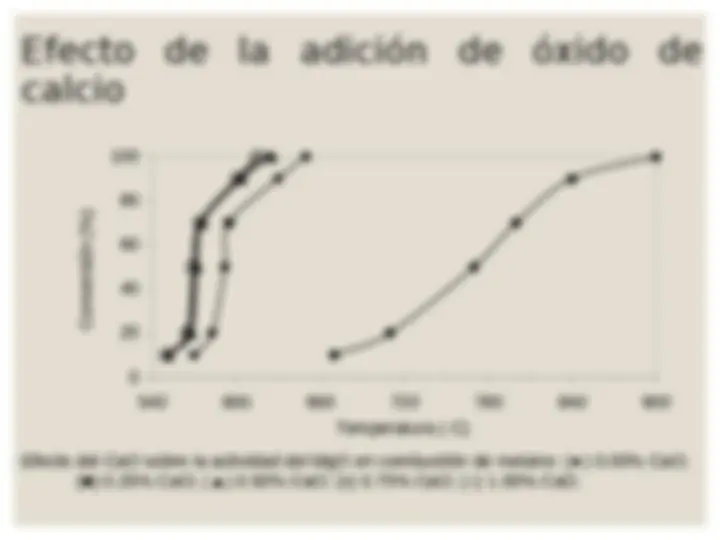
Efecto de la adición de óxido de calcio 100 80 60 40 20 0 540 600 660 720 780 840 900 Temperatura (·C) 2: Efecto del CaO sobre la actividad del MgO en combustión de metano: ( ) 0.00% CaO; (■) 0.25% CaO; (▲) 0.50% CaO; (x) 0.75% CaO; (○) 1.00% CaO. Conversión (%)
Efecto de la temperatura de calcinación 100 80 60 40 20 0 550 580 610 640 Temperatura (°C) Fig. 3: Efecto de la temperatura de calcinación sobre la conversión de metano. Temperatura de calcinación 900°C 1000 °C 1100 °C Conversión (%)